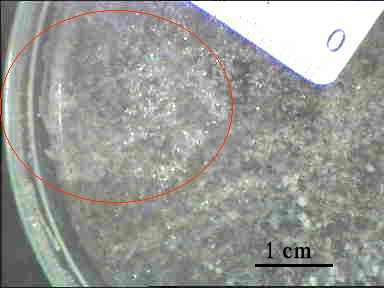
L’eau de mer renferme les ions Na+ et Cl- mais dissous Comment, à partir de cette eau "salée", les cristaux se construisent-ils ?
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
|
La composition de l’eau de mer
n’a
pratiquement pas changé
depuis 3.5 milliards d’années.
Emprisonnés
à
l’origine
à
l’intérieur
de la planète,
la vapeur d’eau
et d’autres
gaz ont fait irruption à
sa surface, créant
ainsi l'atmosphère
terrestre au fur et à
mesure qu’ils
étaient
libérés
par le refroidissement du magma. Après une visite dans le marais salant, nous constatons que le
sel cristallise, et peut ainsi se récolter, à partir d’une
certaine concentration. Nous allons essayer de définir
cette concentration grâce
à
des expériences
faites en sciences –expérimentales.
|
|
Hypothèse |
MISE
EN OEUVRE DES EXPERIENCES I-
1/ Notre
expérience
Afin de produire du sel, nous allons faire bouillir de l’eau
de mer.
Nous utiliserons un bêcher rempli de cette eau. Et nous la ferons
bouillir à l ’aide
d’un
bec bunsen.
Au bout de quelques minutes, l’eau s’étant
évaporée
nous observons un dépôt
blanchâtre
au fond du bêcher
: du sel.

2/Application
à la résolution de notre problème en Biologie
Lors de notre visite au jardin des salines, nous avons prélevé 10
millilitres d’eau
dans chacun des bassins du marais (la réserve, le tour d’eau,
l’hautaie, les brassioux
et les oeillets)
afin de suivre la concentration en sel lors du trajet de l’eau,
de la mer jusqu’au
oeillets.
Dans le premier bêcher, nous avons mis l’eau
de la réserve,
dans le deuxième
celle du tour d’eau,
dans le troisième celle de l’hautaie,
dans le quatrième
l'eau des brassioux, et enfin dans le cinquième
celle des oeillets.
Au bout de quelques instants, nous observons que toute l'eau s'est
évaporée dans chaque bêcher et qu'il ne reste au fond qu'une substance
blanchâtre : Le sel que nous allons peser.

 Dans le premier bêcher, nous remarquons une très faible quantité de sel
: 0,32 grammes.
Dans le premier bêcher, nous remarquons une très faible quantité de sel
: 0,32 grammes.

Observé à la loupe
 Dans le deuxième bêcher où nous avions mis l'eau du tour d'eau, nous
obtenons une plus grande quantité de sel 0.55 grammes.
Dans le deuxième bêcher où nous avions mis l'eau du tour d'eau, nous
obtenons une plus grande quantité de sel 0.55 grammes.

Observé à la loupe
 Nous avons dans le troisième bêcher, contenant l'eau de l'hautaie,
une quantité supérieure au précédent, environ 1,84 grammes.
Nous avons dans le troisième bêcher, contenant l'eau de l'hautaie,
une quantité supérieure au précédent, environ 1,84 grammes.
 Dans le bêcher qui contenait
l'eau des brassioux, nous avons trouvé 2,50 grammes.
Dans le bêcher qui contenait
l'eau des brassioux, nous avons trouvé 2,50 grammes.
 Dans le cinquième où il y
avait l'eau des oeillets, nous avons remarqué une très forte
quantité de sel 3.2 grammes.
Dans le cinquième où il y
avait l'eau des oeillets, nous avons remarqué une très forte
quantité de sel 3.2 grammes.

Observé à la loupe
 Nous pouvons en conclure que
la salinité augmente au fur et à mesure que l'on avance dans le marais
jusqu'à saturation dans les oeillets où le sel cristallise donc lorsque la
concentration atteint une valeur proche de 280 g/L, les sauniers peuvent
récolter le sel ainsi obtenu. Maintenant nous allons vérifier ces
résultats en chimie.
Nous pouvons en conclure que
la salinité augmente au fur et à mesure que l'on avance dans le marais
jusqu'à saturation dans les oeillets où le sel cristallise donc lorsque la
concentration atteint une valeur proche de 280 g/L, les sauniers peuvent
récolter le sel ainsi obtenu. Maintenant nous allons vérifier ces
résultats en chimie.
3/ Notre
expérience en chimie
Grâce à nos échantillons prélevés lors de la visite au jardin des
Salines aux Sables d’Olonne
nous allons pouvoir rechercher la concentration dans chaque bassin.
Afin de réaliser cette expérience, nous prélevons 5 cm3
d’eau
d'un des bassins. Nous plaçons ensuite cette solution dans une fiole jaugée
de 100 cm3, nous remplissons la fiole d'eau distillée afin
d'homogénéiser à cela nous rajoutons enfin 1 mL de
chromate.
Nous prélevons 2 cm3 de la solution que nous plaçons
dans l'erlenmeyer afin de procéder au dosage. Nous versons goutte à goutte du
nitrate d'argent jusqu'à obtention d'une coloration rouge.


Tableau des résultats :
|
Bassins |
1 Réserve |
2 Tour d'eau |
3 Hautaie |
4 Brassioux |
5 oeillet |
|
Calculs
après pesée |
32g/L |
55g/L |
184g/L |
250g/L |
320g/L |
|
Dosage
NaCl |
35g /L |
50,3g/L |
175,5g/L |
250g/L |
292,5g/L |
 Nous confirmons donc que la
concentration augmente au fur et à mesure que l’on avance vers les oeillets. La salinité est
donc de plus en plus élevée jusqu’à
saturation au niveau des oeillets où les
sauniers peuvent alors récolter le sel ainsi obtenu.
Nous confirmons donc que la
concentration augmente au fur et à mesure que l’on avance vers les oeillets. La salinité est
donc de plus en plus élevée jusqu’à
saturation au niveau des oeillets où les
sauniers peuvent alors récolter le sel ainsi obtenu. - Aline,
Christelle, Caroline et Leslie
MISE EN OEUVRE DES EXPERIENCES II-
1/ Expérience
Nous
disposons dans un plateau à fond noir des boîtes de Pétri numérotées de 1à 10
contenant chacune une quantité de sel connue ( on a
versé 25 mL d’eau dans chaque boîte
et pesé
une certaine quantité
de gros sel) :
Le sel s’est
dissout dans l’eau
de chaque boîte.
Seules 3 boîtes
montrent une différence
(boîte
6, 7 et 8).
|
·
Boîte
1 : 35 g/L ·
Boîte
2 : 70 g/L ·
Boîte
3 : 140 g/L ·
Boîte
4 : 200 g/L ·
Boîte
5 : 250 g/L |
·
Boîte
6 : 280 g/L ·
Boîte
7 : 290 g/L ·
Boîte
8 : 300 g/L ·
Boîte
9 : 310 g/L ·
Boîte
10 : 320 g/L |
On couvre les boîtes pour éviter
que l’eau
ne s’évapore
et que les concentrations ne soient modifiées. Le lendemain, on observe que des
cristaux de sel se sont formés dans certaines boîtes.
2/OBSERVATIONS ET RESULTATS
a) Observation à l’oeil nu
Le lendemain, nous constatons que
le sel est resté dissout dans plusieurs boîtes de Pétri. Nous observons les cristaux
de sel non dissout à l’oeil
nu dans les boîtes
6,7 et 8.

zoom
|
|
ABSENCE DE
SEL. 250g/L |
|
|
APPARITION
DE FLEUR DE SEL ET DE CRISTAUX DE SEL. 280g/L |
|
|
QUELQUES
CRISTAUX DE FLEUR DE SEL. 300g/L |
b) Observation à la loupe
binoculaire
A la loupe binoculaire nous avons
l’impression
que les cristaux sont différents selon les boîtes. C’est
ce qui nous pousse à
les observer au microscope.

c) Observation au
microscope
Dans les boîtes 4,5 et 6 de nouveaux
cristaux se sont formés après évaporation d’eau ( 1
semaine après).
La concentration a donc augmenté et a atteint le seuil de cristallisation.
Nous observons les cristaux des boîtes de Pétri 4,5,6
et 8 au microscope. Il y a deux sortes de cristaux. Il y a d'une part des
cristaux parallélipipédiques et d'autre part des
cristaux pyramidaux.
|
|
Exemple de cristaux parallèlépipédiques |
|
|
Exemple de cristaux en trémie |
Les cristaux pyramidaux sont
constitués de cristaux parallèlépipédiques empilés les
uns sur les autres. Ce sont des cristaux de chlorure de sodium.
Conclusion : l’hypothèse
est vérifiée,
les ions en formant la structure cristalline sont tombés au fond et nous avons
donc constaté que le sel cristallise pour une concentration supérieur
à 250 g/L, comprise entre 280 et 300 g/L.
CONCLUSION
Au
fil de nos expériences nous avons pu déterminer la concentration en sel dans
l'eau nécessaire à la récolte. En effet nous avons constaté que pour une
concentration s'approchant de 300 g/L des cristaux de sel apparaissent.
Lorsque l’eau
de mer est très
concentrée
les ions Na+ et Cl- se lient en grande quantité constituant un édifice
cristallin qui au départ flotte (fleur de sel) puis devient trop lourd et tombe
au fond. Il existe une concentration optimale pour laquelle les cristaux se
forment.
Dans le marais, dans la partie où la concentration est de 300 g/L (l'oeillet),
le sel sera récolté
grâce
à
divers instruments :
-
La simouche servira à racler le fond du marais
et regrouper les cristaux à un même endroit
-
et la louse sera utilisée pour ramasser
la fleur de sel.

Sandrine, Estelle, Julien, Kelsey